Aztreonam no causa anafilaxia en pacientes con anafilaxia documentada inducida por penicilina.
Es un blog de Jorge Figueroa Apestegui Medico internista CMP:34170 RNE:031011Hospital Arzobispo Loayza Lima Universidad Nacional Mayor de San Marcos 1990-2004
sábado, 23 de marzo de 2024
El efecto Eagle establece que a medida que el inocolum de los estreptococos del grupo A (GAS) se divide en una fase logarítmica, sus proteínas de unión a penicilina se regulan negativamente. Los agentes activos de la pared celular como la penicilina pueden ser menos efectivos. Esta es una de las razones por las que se administran dosis altas. La terapia con clindamicina se agrega a la penicilina para tratar infecciones necrotizantes graves con GAS o gangrena gaseosa por Clostridium perfringens. La clindamicina puede alterar la síntesis de proteínas y, en teoría, bloquear la producción de toxinas.
viernes, 22 de marzo de 2024
martes, 3 de agosto de 2021
Anticoagulación terapéutica vs profiláctica en COVID-19 Valor del Dimero D
Autor/a: Prof Renato Lopes, Dab Pedro Gabriel Melo de Barros, Silva Remo, et al. Fuente: The Lancet https://doi.org/10.1016/S0140-6736(21)01203-4 Therapeutic versus prophylactic anticoagulation for patients admitted to hospital with COVID-19 and elevated D-dimer concentration (ACTION): an open-label, multicentre, randomised, controlled trial
Aspectos destacados
|
Antecedentes
COVID-19 se asocia con un estado protrombótico que conduce a resultados clínicos adversos. Se desconoce si la anticoagulación terapéutica mejora los resultados en pacientes hospitalizados con COVID-19.
Nuestro objetivo fue comparar la eficacia y seguridad de la anticoagulación terapéutica versus profiláctica en esta población.
Métodos
Hicimos un ensayo pragmático, abierto (con adjudicación ciega), multicéntrico, aleatorizado y controlado, en 31 sitios en Brasil. Los pacientes (≥18 años) hospitalizados con COVID-19 y concentración elevada de dímero D, y que tenían síntomas de COVID-19 durante hasta 14 días antes de la aleatorización, fueron asignados al azar (1: 1) para recibir anticoagulación terapéutica o profiláctica.
La anticoagulación terapéutica fue rivaroxabán oral intrahospitalario (20 mg o 15 mg al día) para pacientes estables, o enoxaparina subcutánea inicial (1 mg / kg dos veces al día) o heparina intravenosa no fraccionada (para lograr una concentración de 0 · 3–0 · 7 UI / mL de concentración anti-Xa) para pacientes clínicamente inestables, seguido de rivaroxabán hasta el día 30.
La anticoagulación profiláctica fue enoxaparina estándar en el hospital o heparina no fraccionada. El resultado primario de eficacia fue un análisis jerárquico del tiempo hasta la muerte, la duración de la hospitalización o la duración del oxígeno suplementario hasta el día 30, analizado con el método del índice de victorias (un índice> 1 refleja un mejor resultado en el grupo de anticoagulación terapéutica) en la intención -población a tratar.
El resultado primario de seguridad fue hemorragia mayor o no mayor clínicamente relevante durante 30 días. Este estudio está registrado en ClinicalTrials.gov (NCT04394377) y está completo.
Resultados
Desde el 24 de junio de 2020 hasta el 26 de febrero de 2021, se seleccionaron 3.331 pacientes y se asignaron aleatoriamente 615 (311 [50%] al grupo de anticoagulación terapéutica y 304 [50%] al grupo de anticoagulación profiláctica). 576 (94%) estaban clínicamente estables y 39 (6%) clínicamente inestables.
Un paciente, en el grupo terapéutico, se perdió durante el seguimiento debido a la retirada del consentimiento y no se incluyó en el análisis primario.
El resultado primario de eficacia no fue diferente entre los pacientes a los que se les asignó anticoagulación terapéutica o profiláctica, con 28 899 (34,8%) victorias en el grupo terapéutico y 34 288 (41,3%) en el grupo profiláctico (proporción de victorias 0,86 [95 % IC 0 · 59–1 · 22], p = 0 · 40).
Se observaron resultados consistentes en pacientes clínicamente estables y clínicamente inestables.
El resultado de seguridad primario de hemorragia mayor o no mayor clínicamente relevante ocurrió en 26 (8%) pacientes a los que se les asignó anticoagulación terapéutica y siete (2%) a las que se les asignó anticoagulación profiláctica (riesgo relativo 3 · 64 [IC 95% 1 · 61–8 · 27 ], p = 0 · 0010).
La reacción alérgica a la medicación del estudio ocurrió en dos (1%) pacientes en el grupo de anticoagulación terapéutica y tres (1%) en el grupo de anticoagulación profiláctica.
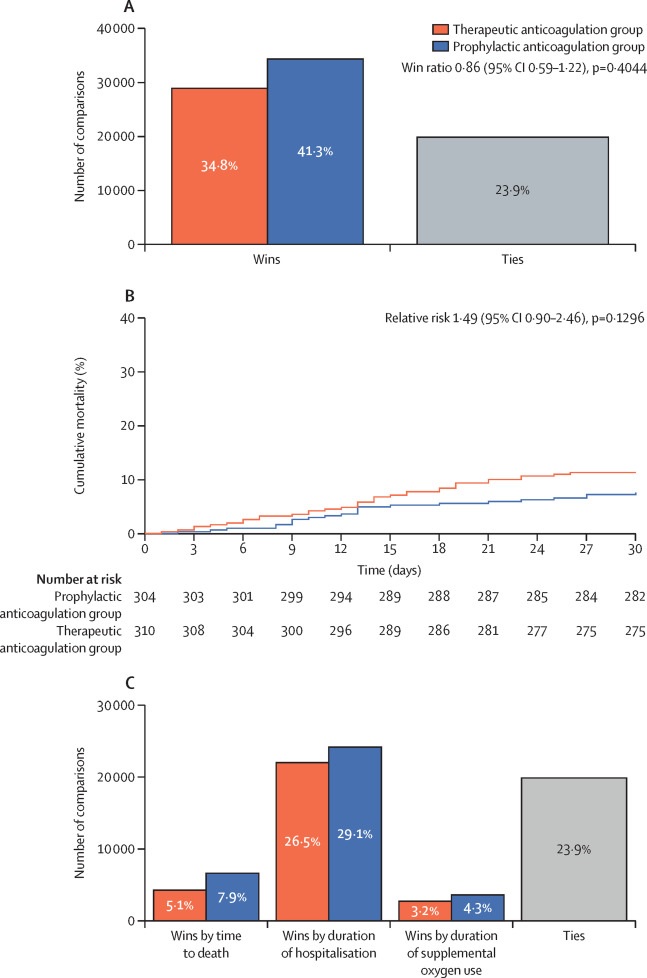
Análisis de resultado primario: (A) Análisis jerárquico del índice de victorias de muerte, duración de la hospitalización y duración del uso de oxígeno (resultado primario) durante 30 días. (B) Curvas de mortalidad acumulada a lo largo de 30 días en los dos grupos de estudio. (C) Número de victorias por grupo para componentes individuales del resultado primario.
Interpretación En pacientes hospitalizados con COVID-19 y concentración elevada de dímero D, la anticoagulación terapéutica intrahospitalaria con rivaroxabán o enoxaparina seguida de rivaroxabán hasta el día 30 no mejoró los resultados clínicos y aumentó el sangrado en comparación con la anticoagulación profiláctica. Por lo tanto, se debe evitar el uso de rivaroxabán en dosis terapéuticas y otros anticoagulantes orales directos en estos pacientes en ausencia de una indicación basada en la evidencia para la anticoagulación oral. |
Investigación en contexto
Evidencia antes de este estudio
COVID-19 se ha asociado con una mayor incidencia y magnitud de complicaciones trombóticas en comparación con otras infecciones respiratorias, y se ha demostrado que la trombosis conduce a peores resultados en estos pacientes. Los estudios observacionales han sugerido que la anticoagulación tanto terapéutica como profiláctica podría estar asociada con una menor mortalidad hospitalaria y una intubación menos frecuente en comparación con ningún tratamiento anticoagulante. Por lo tanto, la anticoagulación terapéutica se ha considerado una opción de tratamiento para los pacientes hospitalizados con COVID-19, sobre la base de evidencia de baja calidad.
Se realizaron búsquedas en MEDLINE, el Registro Cochrane Central de Ensayos Controlados (CENTRAL), Web of Science y Scopus utilizando los términos (“rivaroxaban” O “apixaban” O “dabigatrán” O “edoxabán” O “heparina” O “enoxaparina”) Y (“SARS-CoV-2” O “COVID” O “coronavirus” O “COVID-19”) Y (“aleatorizados” O “ensayos clínicos”), sin restricciones de fecha o idioma. No encontramos ningún ensayo clínico aleatorizado publicado que evalúe los efectos de la anticoagulación terapéutica sobre los resultados clínicos en COVID-19.
Valor agregado de este estudio
Nuestro estudio es el primer ensayo clínico aleatorizado con un tamaño de muestra calculado para evaluar el efecto del uso terapéutico de un anticoagulante oral sobre los resultados clínicos en pacientes hospitalizados con COVID-19 y concentración elevada de dímero D en comparación con la anticoagulación profiláctica.
Los resultados del presente estudio muestran que, en pacientes hospitalizados con COVID-19 y concentración elevada de dímero D, la anticoagulación terapéutica con rivaroxabán en pacientes clínicamente estables y heparina en pacientes clínicamente inestables no mejoró los resultados clínicos ni redujo la muerte, y aumentó el sangrado cuando en comparación con la tromboprofilaxis con heparina.
Nuestro protocolo y plan de análisis estadístico se hicieron públicos y se registraron antes de cerrar la base de datos, y el estudio se diseñó para minimizar el sesgo mediante un protocolo pragmático que se siguió estrictamente. Todos los resultados clínicos, incluidos los eventos hemorrágicos y trombóticos, fueron adjudicados de manera sistemática y centralizada por un comité de eventos clínicos cuyos miembros estaban enmascarados para la asignación de tratamiento.
Proporcionamos descripciones claras y detalladas de los parámetros clínicos y las definiciones de los resultados clínicos. Por lo tanto, nuestro estudio proporciona evidencia de alta calidad para guiar la práctica clínica en un campo donde la mayoría de las decisiones médicas se han tomado sobre la base de evidencia de baja calidad.
Implicaciones de toda la evidencia disponible
Al contrario de lo que se ha demostrado en los datos preliminares con el uso de heparinas, el estudio actual mostró que una estrategia que utiliza principalmente un anticoagulante oral en una dosis terapéutica no resultó en una mejoría clínica de los pacientes hospitalizados con COVID-19.
Debido a que el enfoque de anticoagulación más favorable durante la hospitalización aún no está definido, y se han utilizado muchas estrategias no autorizadas y no basadas en evidencia, nuestros resultados ayudarán a los médicos en el proceso de toma de decisiones al tratar a los pacientes en este entorno clínico.
Financiación: Coalición COVID-19 Brasil, Bayer SA.
Impacto de la Vitamina D oral sobre los marcadores inflamatorios en COVID 19
Autor/a: Lakkireddy, M., Gadiga, S.G., Malathi, R.D. et al. Fuente: Sci Rep 11, 10641 (2021). https://doi.org/10.1038/s41598-021-90189-4 Impact of daily high dose oral vitamin D therapy on the inflammatory markers in patients with COVID 19 disease
Impacto de la terapia diaria con dosis altas de vitamina D oral sobre los marcadores inflamatorios en pacientes con enfermedad por COVID 19
Resumen Se sabe que COVID 19 causa desregulación inmunológica y la vitamina D es un inmunomodulador conocido. Este estudio tiene como objetivo investigar objetivamente el impacto de la terapia Pulse D en la reducción de los marcadores inflamatorios de COVID-19. Se evaluó a los pacientes COVID-19 con hipovitaminosis D consentidos en cuanto a marcadores inflamatorios (relación N / L, PCR, LDH, IL6, ferritina) junto con vitamina D el día 0 y el día 9/11 según su categoría de IMC respectiva. Los sujetos fueron asignados al azar en grupos VD y NVD. El grupo VD recibió terapia Pulse D (suplementación diaria dirigida de 60.000 UI de vitamina D durante 8 o 10 días, dependiendo de su IMC) además del tratamiento estándar. El grupo NVD recibió el tratamiento estándar solo. Se analizaron las diferencias en las variables entre los dos grupos para determinar la significación estadística. Ochenta y siete de los ciento treinta sujetos han completado el estudio (VD: 44, NVD: 43). El nivel de vitamina D aumentó de 16 ± 6 ng / ml a 89 ± 32 ng / ml después de la terapia con Pulso D en el grupo VD y se observó una reducción muy significativa (p <0,01) de todos los marcadores inflamatorios medidos. La reducción de marcadores en el grupo NVD fue insignificante (p> 0.05). La diferencia en la reducción de marcadores entre los grupos (NVD vs VD) fue muy significativa (p <0,01). La mejora terapéutica de la vitamina D a 80-100 ng / ml ha reducido significativamente los marcadores inflamatorios asociados con COVID-19 sin efectos secundarios. Por lo tanto, la terapia complementaria Pulse D se puede agregar de manera segura a los protocolos de tratamiento existentes de COVID-19 para obtener mejores resultados. |
Introducción
La pandemia COVID-19 causada por el virus SARS-CoV-2 ha creado una dificultad sin precedentes en los últimos tiempos. Las consecuencias graves de COVID-19 se atribuyeron a la desregulación inmunitaria que condujo a una mayor producción de mediadores proinflamatorios (tormenta de citocinas).
En ausencia de una vacuna o un tratamiento específicos, las estrategias para minimizar los efectos del COVID-19 se han vuelto extremadamente importantes. Estudios observacionales recientes han informado que los pacientes con niveles más altos de vitamina D en suero (vitamina D) tenían síntomas menos graves y viceversa y han postulado la utilidad de la vitamina D en la prevención y el tratamiento de COVID-19. Se atribuyó a los efectos beneficiosos de la vitamina D en COVID-19 que estaban mediados por sus múltiples acciones sobre el sistema inmunológico.
Se sabe que la vitamina D mejora la producción de varios péptidos antimicrobianos por las células inmunitarias y la vitamina D modula el sistema inmunológico de acuerdo con el medio interno. Reduce la producción desregulada de citocinas proinflamatorias autodestructivas y promueve la expresión de citocinas antiinflamatorias por parte de las células inmunes. El papel dinámico de la vitamina D puede ser de gran valor en el contexto de la disfunción inmune observada en pacientes con COVID-19 con tormenta de citocinas y síndrome de dificultad respiratoria aguda.
Aunque los efectos inmunomoduladores protectores de la vitamina D se exploraron en muchas enfermedades autoinmunes e infecciones del tracto respiratorio, existe una escasez de información de los ensayos clínicos aleatorios en COVID-19.
La terapia de pulso de vitamina D es un enfoque dirigido a aumentar el nivel de vitamina D en suero mediante el uso de dosis altas (60.000 UI) de suplementos orales de vitamina D diariamente durante un período de tiempo específico determinado por el IMC del individuo, el nivel inicial de vitamina D y la formulación.
Este estudio tiene como objetivo investigar objetivamente el papel de la vitamina D y el impacto de la terapia Pulse D en la reducción de los biomarcadores inflamatorios de COVID-19.
Material y métodos
Se trata de un ensayo clínico intervencionista, prospectivo, aleatorizado, de etiqueta abierta, de asignación paralela, que se llevó a cabo en el Gandhi Medical College, Hospital Secunderabad, en colaboración con el Instituto de Ciencias Médicas de Nizam, Hyderabad, después de recibir la aprobación del comité de ética institucional.
Se obtuvo el consentimiento informado por escrito de todos los sujetos y se siguieron todas las normas y reglamentos pertinentes. Pacientes confirmados de COVID-19 mayores de 18 años con hipovitaminosis D (nivel de vit D por debajo de 30 ng / ml) y enfermedad leve a moderada (SpO2> 90%) según las directrices revisadas para COVID-19 emitidas por la Dirección General of Health Services, Government of India el 31-03-2020 fueron incluidos.
Se excluyeron pacientes con enfermedad grave y pacientes que hayan tomado altas dosis de vitamina D (60.000 UI) en los últimos 3 meses, pacientes con malignidad activa, enfermedad renal crónica y VIH, madres embarazadas y lactantes.
Después de la admisión, a los pacientes con enfermedades leves a moderadas se les asignaron los números de serie y se les examinó el nivel de vitamina D sérica junto con los marcadores inflamatorios de COVID-19.
Los pacientes con hipovitaminosis D se asignaron al azar en dos grupos frente al grupo experimental / grupo vit.D (grupo VD) y el grupo de control / comparador activo (grupo NVD) alternativamente según sus números de serie previos a la asignación. Los sujetos del grupo VD recibieron terapia complementaria Pulse D (60.000 UI de vitamina D en forma de nano solución acuosa (Deksel) por día durante 8 días para sujetos con índice de masa corporal (IMC) de 18-25 y 10 días para sujetos con IMC> 25) junto con el tratamiento estándar de rutina para COVID-19. Los sujetos del grupo NVD recibieron tratamiento estándar para COVID-19 solo.
Después de completar el tratamiento con vitamina D, se recogieron muestras de suero repetidas para la vitamina D y los marcadores inflamatorios en el día 9 o 11, respectivamente, para el grupo VD. De manera similar, se recolectaron muestras el noveno día para pacientes con IMC de 16-25 y el undécimo día para pacientes con IMC> 25 en el grupo NVD.
Los sujetos de ambos grupos (VD y NVD) que no habían recibido medicamentos como Remdesivir, Favipiravir, Ivermectina o Dexametasona se subcategorizaron en subgrupos de eVD y eNVD. En estos subgrupos se estudió el papel exclusivo de la vitamina D (sin la influencia de fármacos antivirales o corticosteroides) en la reducción de los marcadores inflamatorios de COVID-19.
Resultados
Se incluyeron ciento treinta sujetos confirmados con COVID-19 y 87 sujetos pudieron completar el estudio. La edad media de los pacientes que completaron el estudio (n = 87) fue de 45 ± 13 años, rango de 20 a 83 años. La edad media de los pacientes en el grupo VD (n = 44) fue 47 ± 12 años, rango 20-70 años y en el grupo NVD (n = 43) fue 44 ± 14 años, rango 20-83 años. No hubo diferencia significativa en la edad entre los dos grupos (p = 0,23).
No hubo diferencias significativas en la mediana del IMC entre los pacientes de los grupos VD (25) y NVD (24) (Z = - 0,8, p = 0,4). No hubo diferencias significativas en la duración media de los síntomas entre los pacientes de los grupos VD (5 días) y NVD (5 días) (Z = 0,9, p = 0,4).
No hubo diferencia significativa (p> 0.05) en los parámetros vitales entre los grupos NVD y VD (presión arterial sistólica media: p = 0,9, presión arterial diastólica media: p = 0,4, frecuencia cardíaca mediana: p = 0,3, SpO2 mediana: p = 0.8) en el momento de la inscripción.
34 de los 87 sujetos que completaron el estudio tenían diabetes o hipertensión como comorbilidad (39%). Debido a la asignación al azar, 21 y 13 sujetos con comorbilidades fueron asignados al grupo VD y NVD respectivamente. No hubo diferencia significativa (p> 0,05) en los niveles de todos los marcadores inflamatorios medidos en los sujetos de ambos grupos con y sin comorbilidades antes y después del tratamiento.
De los 87 sujetos que completaron el estudio, el 75% (n = 65) eran hombres y el 25% (n = 22) eran mujeres. Debido a la asignación al azar n = 37, 28 hombres yn = 7, se asignaron 15 mujeres a los grupos VD y NVD respectivamente.
La diferencia en los marcadores inflamatorios antes del tratamiento entre los géneros en los grupos VD y NVD no fue significativa (p> 0.05) excepto para IL6 (p = 0.02) en el grupo VD y Ferritina (p = 0.002) en el grupo NVD con los hombres con niveles más altos.
La diferencia en los marcadores inflamatorios después del tratamiento entre los géneros en los grupos VD y NVD no fue significativa (p> 0,05) excepto por una PCR más alta (p = 0,02) en las mujeres y una mayor ferritina (p = 0,002) en los hombres del grupo NVD.
La diferencia en la reducción de los marcadores inflamatorios entre los dos grupos (NVD frente a VD) fue muy significativa (p <0,01), siendo la reducción en el grupo de VD notablemente más alta que en el grupo de NVD.
(haga clic sobre la imagen para ampliarla)

La diferencia en la estancia hospitalaria media entre los grupos VD vs NVD (13 ± 5 días frente a 14 ± 5 días) no fue significativa (p = 0,9).
Se requirió apoyo en cuidados intensivos para 9 sujetos (grupo VD: n = 4, grupo NVD: n = 5) y 7 de ellos murieron (grupo VD: n = 2, grupo NVD: n = 5). 6 de estos 7 sujetos (grupo VD: n = 2, grupo NVD: n = 4) murieron después de 5 ± 1 día de inscripción sin completar el estudio. Un sujeto en el grupo NVD murió después de 21 días de inscripción. Todos tenían niveles muy altos de marcadores inflamatorios al ingreso en comparación con los supervivientes.
La diferencia fue altamente significativa (p <0.01) para IL6, CRP, Ferritina y significativa (p = 0.02) para la relación N / L y LDH. 2 de los 7 sujetos que no sobrevivieron (28,5%) tenían diabetes o hipertensión como comorbilidad.
No se observaron reacciones adversas atribuibles a la toxicidad de la vitamina D en ninguno de los pacientes estudiados. El nivel de calcio sérico en el grupo VD después del tratamiento estaba dentro de los límites normales (9 ± 0,5 mg / dl).
Discusión
El COVID-19 causado por el SARS-CoV-2 (nuevo virus corona) no solo ha provocado una intensa respuesta inmune adaptativa en las personas que se vieron afectadas por él, sino que también ha provocado una inmensa respuesta humana en varios frentes para combatirlo en todo el mundo. Como la desregulación inmune causada por COVID-19 conduce a insuficiencia respiratoria y síndrome de disfunción multiorgánica, se hicieron muchos intentos para reutilizar los medicamentos disponibles para abordar los desafíos planteados por el nuevo virus corona.
Se registró una alta mortalidad y morbilidad en pacientes con marcadores inflamatorios significativamente elevados (marcadores sustitutos de la gravedad de COVID-19) como la relación N / L, PCR, LDH, IL6, ferritina, dímero D, etc. De manera similar, también se registró una alta mortalidad y morbilidad en pacientes con deficiencia de vitamina D. Se propuso un nivel bajo de vitamina D como un factor de riesgo independiente para adquirir infección por COVID-19, hospitalización y mortalidad relacionada con COVID-19.
Con base en la evidencia anterior de que la vitamina D podría disminuir la incidencia de la gripe y otras infecciones respiratorias y los estudios observacionales en COVID-19, se han publicado pocas hipótesis y recomendaciones en apoyo de complementar la vitamina D para evitar las graves consecuencias de COVID- 19. Kaufman y col. informaron que la positividad para el SARS-CoV-2 está asociada fuerte e inversamente con el nivel sérico de vitamina D y propuso que la suplementación con vitamina D podría reducir el riesgo de infección por SARS-CoV-2 y enfermedad por COVID-19.
La vitamina D tiene innumerables efectos sobre la fisiología humana. Además de sus efectos musculoesqueléticos endocrinos y calcitrópicos, es un inmunomodulador potencial. Dependiendo del medio interno predominante y el nivel de 25 hidroxi vitamina D en la sangre, la activación intracrinal de la 1α hidroxilasa ocurre en las células inmunes para producir calcitriol localmente y tener sus efectos autocrinos como la promoción de la respuesta inmune innata a las infecciones y la modulación del sistema inmunológico adaptativo. respuesta.
Vit.D actúa como un interruptor inteligente para disminuir la respuesta Th1 y las citocinas proinflamatorias mientras mejora la producción de citocinas antiinflamatorias en casos de desregulación inmune. Es pertinente señalar que el virus SARS-CoV-2 activa la respuesta Th1 y suprime la respuesta Th24. Se postuló que los niveles de vitamina D por encima de 40-60 ng / ml podrían ser protectores para superar la crisis de COVID-19. Annweiler y col. informaron que los pacientes ancianos frágiles hospitalizados que habían tomado regularmente suplementos de vitamina D en bolo antes de la hospitalización con COVID-19 tenían tasas de supervivencia significativamente mejores que otros.
Aún no se han completado ni informado pocos ensayos controlados aleatorios que utilicen dosis en bolo de vitamina D en COVID-19. McNally y col. informaron que se puede lograr una rápida normalización de los niveles de vitamina D con la terapia de carga, teniendo debidamente en cuenta el estado de la enfermedad, el nivel basal de vitamina D y el peso, pero se recomienda evitar las dosis de carga > 300 000 UI hasta que se realicen ensayos para evaluar el riesgo y beneficio. Las terapias con dosis de bolo intermitente vit.D con intervalos de 3 meses no han logrado alcanzar los niveles objetivo.
Como se conocen los efectos dependientes de la concentración de la vitamina D sobre el sistema inmunológico y los medios para alcanzar dichas concentraciones de forma segura en el menor tiempo posible en un individuo determinado, hemos realizado este estudio para determinar el impacto de la terapia Pulse D sobre los marcadores inflamatorios de COVID-19.
Los dos grupos aleatorizados de nuestro estudio se emparejaron con respecto a la edad, el IMC, la duración de los síntomas, las comorbilidades y los parámetros vitales. A pesar de la coincidencia de varios parámetros, la diferencia significativa en los marcadores antes del tratamiento entre los grupos fue intrigante. Esta diferencia se puede atribuir solo al azar. Se observó un predominio masculino (75% vs 25%) similar a informes anteriores.
El análisis de los marcadores inflamatorios antes y después del tratamiento en el grupo VD ha mostrado una reducción muy significativa (p <0,01) en todos los marcadores inflamatorios después de la terapia complementaria con pulso D. Por el contrario, se observó una reducción insignificante (p> 0,05) de los marcadores inflamatorios en el grupo de NVD.
La diferencia en la reducción de los marcadores inflamatorios entre los grupos (NVD frente a VD) fue muy significativa (p <0,01) y la reducción de los marcadores fue marcadamente alta en el grupo de VD en comparación con el grupo de NVD. Por lo tanto, la terapia complementaria con pulso D dirigida a un nivel medio de vit D de 80-100 ng / ml ha reducido eficazmente los marcadores inflamatorios asociados con la tormenta de citocinas y la gravedad de COVID-19.
En nuestro estudio se observó una reducción significativa de la PCR en comparación con el informe de Rastogi et al. Esto puede atribuirse a la diferencia en el nivel de vitamina D después del tratamiento. Según nuestro conocimiento, estos hallazgos son los primeros de este tipo que se informan.
Hemos analizado los marcadores inflamatorios en un subconjunto separado de casos (subgrupos de eVD y eNVD) derivados de ambos grupos de estudio que no han recibido ningún fármaco como Remdesivir, Favipiravir o Ivermectina o Dexametasona. Se observó una reducción muy significativa (p <0,01) en todos los marcadores inflamatorios medidos con un aumento significativo de la vit.D en el subgrupo de eVD, a diferencia del subgrupo de eNVD (p> 0,05). La diferencia en la reducción de los marcadores inflamatorios entre los subgrupos (eNVD frente a eVD) fue muy significativa (p <0,01), siendo la reducción de marcadores marcadamente alta en el subgrupo de eVD en comparación con el subgrupo de eVD.
Por lo tanto, se ha demostrado que la mejora en el nivel sérico de vitamina D a 80 ng / ml reduce eficazmente los niveles de marcadores sustitutos de la gravedad de COVID-19 / tormenta de citocinas de forma independiente. Estos hallazgos son exclusivos de nuestro estudio hasta la fecha y no se pueden comparar con otros.
DiNicolantonio y col. informó que tanto el magnesio como la vitamina D son importantes para el sistema inmunológico de forma independiente. Juntos, pueden ser beneficiosos en la infección por COVID-19, ya que el magnesio es necesario para activar la vitamina D. Los resultados de nuestro estudio se pueden comparar con los resultados de estudios futuros con y sin magnesio en regímenes de alta dosis de vitamina D para formular esquemas de dosificación eficaces
La estancia hospitalaria fue subjetiva y multifactorial en ambos grupos. No puede atribuirse únicamente al impacto físico de la enfermedad. Murai y col. informaron que una sola dosis alta de vitamina D3 (200 000 UI) no ha reducido significativamente la duración de la estancia hospitalaria, la mortalidad o la admisión en la UCI en comparación con el placebo. Sus hallazgos no respaldaron el uso de una dosis única en bolo de vitamina D3 para el tratamiento del COVID-1935 de moderado a grave.
En el momento de la inscripción, se observaron niveles significativamente más altos de todos los marcadores inflamatorios en los no supervivientes en comparación con los supervivientes. Jain et al., describieron una relación similar entre la mortalidad y los niveles elevados de marcadores inflamatorios. en su estudio observacional.
En nuestro estudio no se informaron reacciones adversas a la vitamina D. Los niveles de calcio sérico estuvieron dentro de los límites normales después del tratamiento (9 ± 0,5 mg / dl) en el grupo de VD. Rastogi et al. ya largo plazo por McCullough et al. De Carvalho y col. reportaron que las mega dosis (6,00,000 UI) de vitamina D administradas por vía intramuscular incluso en casos de nefrolitiasis son seguras.
Conclusiones
|
COVID-19 y dislipidemia aterogénica
Autor/a: Alfonso Bellia, Aikaterini Andreadi, Luca Giudice, Sofia De Taddeo, et al. Fuente: Diabetes Care 2021 Jul; dc202838. https://doi.org/10.2337/dc20-2838 Atherogenic Dyslipidemia on Admission Is Associated With Poorer Outcome in People With and Without Diabetes Hospitalized for COVID-19
Introducción
La pandemia de la enfermedad por coronavirus 2019 (COVID-19) representa uno de los mayores desafíos de salud pública en los últimos años. La identificación de factores de riesgo de mal pronóstico de COVID-19 es una tarea clave para minimizar la morbilidad y la mortalidad atribuibles a la enfermedad.
Se han informado varias anomalías metabólicas en pacientes con COVID-19 confirmado, a menudo relacionadas con la gravedad de la enfermedad, lo que genera la hipótesis de un papel putativo en la patogénesis del síndrome respiratorio agudo severo por coronavirus 2 (SARSCoV-2). En consecuencia, se informa en gran medida que los pacientes con diabetes con COVID-19, especialmente cuando se asocia la obesidad, tienen un mayor riesgo de morir o requerir cuidados intensivos.
En general, la hiperglucemia crónica es un predictor independiente de mal pronóstico en las infecciones del tracto respiratorio inferior, especialmente cuando ya han ocurrido complicaciones micro y macrovasculares establecidas. La evidencia disponible demuestra que la diabetes es un factor de riesgo clave para las enfermedades infecciosas y que las personas con diabetes tienen un mayor riesgo de mortalidad relacionada con la infección.
Aparte de la falta de control de la glucosa y las complicaciones coexistentes de la diabetes, que necesariamente contribuyen a la predisposición inherente a la enfermedad de los pacientes con diabetes, la resistencia a la insulina concomitante puede acompañar a las formas graves de COVID-19 porque la resistencia a la insulina está estrechamente relacionada con la inflamación sistémica, estado protrombótico , disfunción vascular y alteración de la respuesta inmunitaria. En conjunto, estas anomalías fisiopatológicas contribuyen potencialmente al estado de sobreinflamación metabólica informado en pacientes con curso más severo de COVID-19.
Aunque el conocimiento sobre la resistencia a la insulina podría ser útil para mejorar la evaluación del riesgo de un curso complicado de la enfermedad en pacientes con COVID-19 grave, su medición directa no es fácil de realizar en la práctica clínica o, especialmente, en el ámbito hospitalario. Además del sobrepeso, una característica común fuertemente relacionada con la insulina y la llamada dislipidemia aterogénica, es decir, la co-ocurrencia de hipertrigliceridemia, HDL bajo y partículas LDL pequeñas y densas.
Objetivo
Identificar los factores metabólicos asociados con la enfermedad crítica puede ayudar a mejorar el manejo de los pacientes hospitalizados por coronavirus 2019 (COVID-19). Los triglicéridos altos y los niveles bajos de HDL caracterizan la dislipidemia aterogénica estrechamente relacionada con la resistencia a la insulina y la diabetes.
Examinamos las asociaciones de dislipidemia aterogénica detectada en la admisión con el resultado de COVID-19 durante la hospitalización.
Metodología
Analizamos retrospectivamente los informes clínicos de 118 pacientes consecutivos hospitalizados por COVID-19 en Roma, Italia, entre marzo y mayo de 2020. Se recogieron las características clínicas, los marcadores de inflamación y los parámetros del metabolismo de la glucosa y los lípidos al ingreso.
La enfermedad crítica se definió como la muerte intrahospitalaria o la necesidad de intubación endotraqueal. Las asociaciones se probaron mediante análisis de regresión logística.
Resultados
Los pacientes con COVID-19 crítico (n = 43) eran significativamente mayores que aquellos con enfermedad no crítica (n = 75) y presentaban niveles más altos de glucosa en ayunas, triglicéridos, proteína C reactiva, interleucina-6, procalcitonina y dímero d (P <0.01 para todos), mientras que los niveles de HDL fueron más bajos (P = 0.003).
La dislipidemia aterogénica fue más frecuente en pacientes con COVID-19 crítico (46 vs.24%, P = 0.011), así como diabetes (37 vs.19%, P = 0.026), y se asoció significativamente con muerte o intubación (odds ratio 2,53 [IC del 95%: 1,16–6,32], p = 0,018).
Los triglicéridos se asociaron significativamente con biomarcadores inflamatorios seleccionados (P <0,05 para todos) y un peor resultado de COVID-19 durante la hospitalización tanto en la población general como en el subgrupo con dislipidemia aterogénica.
Discusión
En el estudio actual, informamos una asociación significativa entre la detección de dislipidemia aterogénica al ingreso y el resultado adverso posterior de la enfermedad en pacientes hospitalizados por COVID-19. Más específicamente, la dislipidemia aterogénica estuvo fuertemente relacionada con la mortalidad, lo que resultó en más de tres veces mayor probabilidad de asociación con muerte intrahospitalaria (OR 3,63 [IC 95% 1,24–5,77]; P = 0,009).
Los niveles de triglicéridos detectados al ingreso también se asociaron positivamente con los niveles de PCR, procalcitonina y dímero D, que a su vez fueron más altos en pacientes con COVID-19 crítico.
La presencia de niveles altos de triglicéridos es frecuente en la diabetes tipo 2 y está estrechamente relacionada con la resistencia a la insulina.
Actualmente se ha establecido que los pacientes con diabetes preexistente, especialmente si se asocia con obesidad y otras comorbilidades relacionadas, tienen un alto riesgo de muerte o de hospitalización prolongada y complicada por COVID-19, según lo informado por varios grandes estudios retrospectivos de diferentes áreas geográficas. En nuestra población más pequeña, confirmamos la presencia de diabetes como el principal factor de gravedad de la enfermedad, con una prevalencia general de casi el 25%, que no es diferente de la prevalencia estandarizada por edad de la diabetes informada en Italia.
Curiosamente, la glucosa en ayunas al ingreso (mmol / L), pero no los niveles de HbA1c, resultó estar relacionada con la muerte intrahospitalaria o la intubación por dificultad respiratoria (OR 1,11 [IC 95% 1,02-1,43], P = 0,026). Tal asociación podría ser bidireccional. De hecho, la hiperglucemia en sí misma puede afectar directamente las defensas del huésped, incluida la función de granulocitos y macrófagos, y amplificar la respuesta hiperinmune asociada con COVID-19 grave.
Alternativamente, el aumento de la glucosa en sangre podría ser el resultado del estrés metabólico determinado por una infección más grave. Por el contrario, los niveles de HbA1c no fueron diferentes entre los pacientes con peores o mejores resultados, mientras que la prevalencia de diabetes entre los pacientes fue significativamente mayor para los grupos con peor pronóstico (37 frente a 19%, P = 0,026). Estos hallazgos no son fáciles de interpretar.
Según las historias clínicas hospitalarias, no surgieron diferencias sustanciales entre los pacientes con diabetes con COVID-19 crítico y no crítico en cuanto a edad, sexo y tratamiento antihiperglucémico previo al ingreso. En particular, la terapia con insulina de rutina antes del ingreso, que se ha asociado con mortalidad en otra cohorte hospitalizada por COVID-19, no fue diferente entre los grupos de nuestra población. Lamentablemente, no se dispuso de información sobre las complicaciones microvasculares, que habría sido útil para definir mejor la gravedad de la diabetes.
En conclusión, nuestro estudio proporciona evidencia por primera vez de que la dislipidemia aterogénica detectada al ingreso, y en particular la hipertrigliceridemia, puede ser otra anomalía metabólica independiente asociada con pronóstico adverso en pacientes hospitalizados con COVID-19, que merece ser investigado más en poblaciones más grandes . Por lo tanto, debe fomentarse la evaluación del perfil lipídico, junto con otros factores de riesgo ya establecidos, en pacientes con COVID-19 grave.
Mensajes finales
|
Lesión pulmonar autoinfligida en pacientes con COVID-19
Autor/a: Weaver, L., Das, A., Saffaran, S. et al. Fuente: Ann. Intensive Care 11, 109 (2021). https://doi.org/10.1186/s13613-021-00904-7 High risk of patient self-inflicted lung injury in COVID-19 with frequently encountered spontaneous breathing patterns
Resumen Antecedentes Existe una controversia en curso con respecto a la posibilidad de que un mayor esfuerzo respiratorio genere una lesión pulmonar autoinfligida por el paciente (P-SILI) en pacientes que respiran espontáneamente con insuficiencia respiratoria hipoxémica aguda COVID-19. Sin embargo, la evidencia clínica directa que relacione el aumento del esfuerzo inspiratorio con la lesión pulmonar es escasa. Adaptamos un simulador computacional de fisiopatología cardiopulmonar para cuantificar las fuerzas mecánicas que podrían conducir a P-SILI en diferentes niveles de esfuerzo respiratorio. De acuerdo con datos recientes, los parámetros del simulador se ajustaron manualmente para generar una población de 10 pacientes que recapitulan las características clínicas exhibidas por ciertos pacientes con COVID-19, es decir, hipoxemia severa combinada con una mecánica pulmonar relativamente bien conservada, siendo tratados con oxígeno suplementario. Resultados Las simulaciones se realizaron a volúmenes corrientes (VT) y frecuencias respiratorias (RR) de 7 ml / kg y 14 respiraciones / min (que representan el esfuerzo respiratorio normal) y a VT / RR de 7/20, 7/30, 10/14, 10 / 20 y 10/30 ml / kg / respiraciones / min. Si bien la oxigenación mejoró con mayores esfuerzos respiratorios, se observaron aumentos significativos en múltiples indicadores de la posibilidad de lesión pulmonar en todas las combinaciones más altas de VT / RR probadas. La oscilación de la presión pleural aumentó de 12,0 ± 0,3 cmH2O al inicio a 33,8 ± 0,4 cmH2O a VT / RR de 7 ml / kg / 30 respiraciones / min y a 46,2 ± 0,5 cmH2O a 10 ml / kg / 30 respiraciones / min. La oscilación de la presión transpulmonar aumentó de 4,7 ± 0,1 cmH2O al inicio a 17,9 ± 0,3 cmH2O a VT / RR de 7 ml / kg / 30 respiraciones / min y a 24,2 ± 0,3 cmH2O a 10 ml / kg / 30 respiraciones / min. La tensión pulmonar total aumentó de 0,29 ± 0,006 al inicio del estudio a 0,65 ± 0,016 a 10 ml / kg / 30 respiraciones / min. La potencia mecánica aumentó de 1,6 ± 0,1 J / min al inicio a 12,9 ± 0,2 J / min a VT / RR de 7 ml / kg / 30 respiraciones / min, y a 24,9 ± 0,3 J / min a 10 ml / kg / 30 respiraciones / min. La presión de conducción aumentó de 7,7 ± 0,2 cmH2O al inicio a 19,6 ± 0,2 cmH2O a VT / RR de 7 ml / kg / 30 respiraciones / min y a 26,9 ± 0,3 cmH2O a 10 ml / kg / 30 respiraciones / min. Conclusiones Nuestros resultados sugieren que las fuerzas generadas por el aumento del esfuerzo inspiratorio que se observa comúnmente en la insuficiencia respiratoria hipoxémica aguda COVID-19 son comparables con las que se han asociado con la lesión pulmonar inducida por el ventilador durante la ventilación mecánica. Los esfuerzos respiratorios en estos pacientes deben monitorearse y controlarse cuidadosamente para minimizar el riesgo de lesión pulmonar. |
Comentarios
Investigadores de la Universidad de Warwick han investigado el impacto de los esfuerzos respiratorios elevados en los pulmones de pacientes que padecen insuficiencia respiratoria aguda debido a COVID-19, quienes evaluaron la probabilidad de una lesión pulmonar resultante.
Universidad de Warwick
- Algunos pacientes con COVID-19 que experimentan insuficiencia respiratoria aguda responden aumentando significativamente su esfuerzo respiratorio, respirando más rápido y más profundamente.
- Algunos médicos se preocupan de que este nivel de esfuerzo respiratorio pueda provocar más daños en los pulmones de estos pacientes.
Trabajando con un equipo internacional de médicos de cuidados intensivos líderes, los investigadores de ingeniería de la Universidad de Warwick han utilizado modelos computacionales para proporcionar nueva evidencia de que los esfuerzos respiratorios elevados en pacientes con COVID-19 pueden producir presiones y tensiones dentro del pulmón que pueden resultar en lesiones.
Investigadores de la Universidad de Warwick han investigado el impacto de los esfuerzos respiratorios elevados en los pulmones de pacientes que padecen insuficiencia respiratoria aguda debido a COVID-19, quienes evaluaron la probabilidad de una lesión pulmonar resultante.
Aunque la ventilación mecánica es una intervención que salva vidas, la posibilidad de que los ventiladores mecánicos dañen aún más los pulmones ya enfermos al aplicar presiones y fuerzas excesivas es ahora bien reconocida entre los médicos de cuidados intensivos, que implementan protocolos específicos para minimizar el riesgo de los llamados ventiladores. lesión pulmonar inducida.
Desde el comienzo de la pandemia actual, algunos médicos han argumentado que lesiones similares podrían producirse por un mayor esfuerzo respiratorio en pacientes con COVID-19 que respiran espontáneamente.
La llamada lesión pulmonar autoinfligida por el paciente es un concepto controvertido en la comunidad de cuidados intensivos, y algunos médicos insisten en que no hay evidencia de su existencia, mientras que otros argumentan que los pacientes deben, si es necesario, colocarse en ventiladores mecánicos para evitarlo.
Existe un debate en curso sobre el potencial de un aumento de los esfuerzos respiratorios para generar una lesión pulmonar autoinfligida por el paciente en pacientes que respiran espontáneamente con insuficiencia respiratoria hipoxémica aguda COVID-19, sin embargo, la evidencia clínica directa que vincula el aumento del esfuerzo inspiratorio con la lesión pulmonar es escasa.
En el artículo, 'Alto riesgo de lesión pulmonar autoinfligida por el paciente en COVID-19 con patrones de respiración espontánea encontrados con frecuencia: un estudio de modelado computacional', publicado en la revista Annals of Intensive Care, investigadores de la Universidad de Warwick han adaptado un simulador de fisiopatología cardiopulmonar para cuantificar las fuerzas mecánicas que pueden conducir a una lesión pulmonar autoinfligida por el paciente, a diferentes niveles de esfuerzo respiratorio.
El simulador se configuró para representar una población de 10 pacientes con COVID-19, en tratamiento con oxígeno suplementario.
Para cada uno de estos pacientes, se probaron simulaciones en un rango de volúmenes tidales (profundidad de la respiración) y frecuencias respiratorias, desde un volumen tidal de 7 ml / kg y una frecuencia respiratoria de 14 respiraciones por minuto (que representa la respiración normal), hasta un volumen corriente de 10 ml / kg y frecuencia respiratoria de 30 respiraciones por minuto (lo que representa un esfuerzo respiratorio elevado).
Los resultados de las simulaciones indicaron que se podrían generar presiones y tensiones potencialmente dañinas a niveles de esfuerzo respiratorio que los médicos ven con frecuencia en los pacientes con COVID-19.
El profesor Declan Bates, de la Escuela de Ingeniería de la Universidad de Warwick comenta:
"Nuestro modelo ha encontrado que los pacientes que experimentan insuficiencia respiratoria hipoxémica aguda COVID-19 pueden tener un riesgo significativo de lesión pulmonar autoinfligida por el paciente debido al aumento de los esfuerzos respiratorios. Estos esfuerzos deben ser monitoreados y controlados cuidadosamente durante su atención".
"Los pacientes siempre deben seguir los consejos de sus médicos con respecto al momento de inicio del soporte de oxígeno, la ventilación no invasiva o la ventilación mecánica".
